安定供給
安定供給は医療用医薬品に課せられた使命の一つ。
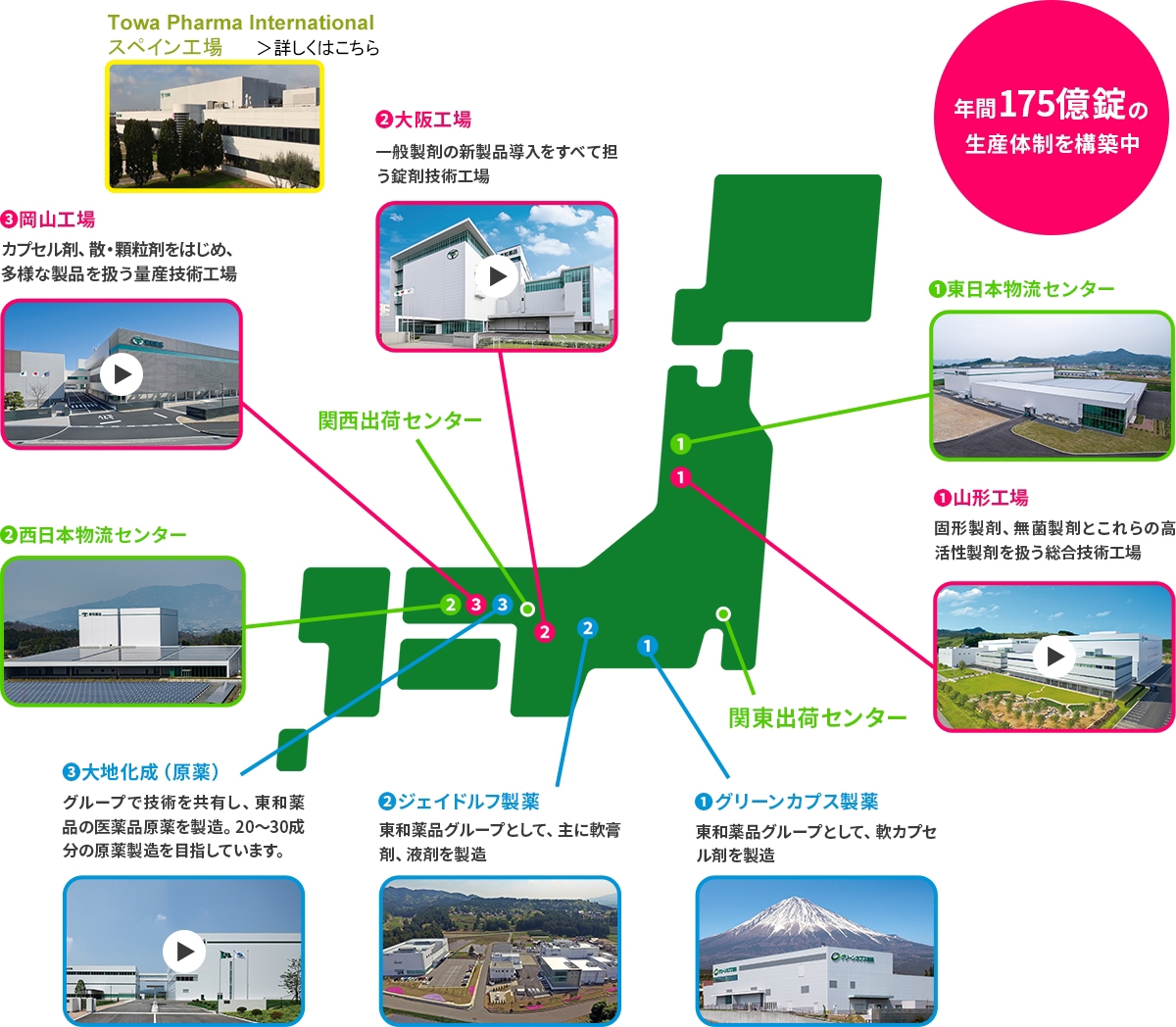
東和薬品は、原薬を複数の原薬メーカーから調達する取り組み(複数購買化)、グループ会社の大地化成における原薬の製造(自製化)を進める等、原薬調達におけるリスク管理を行っています。
また、国内3工場によるバックアップ体制によって万一どこかの工場が操業停止した場合でも、他の工場で補完できる体制を目指しています。新たに連結子会社であるTowa Pharma International Holdings, S.L.のスペイン工場において日本国内向け製造も開始いたしました。これらによりグループとして強固な生産バックアップ体制を構築していきます。
グループ会社であるジェイドルフ製薬では主に軟膏剤、液剤、グリーンカプス製薬では軟カプセル剤を製造しており、多様な剤形に対応した生産体制を構築しています。

東和薬品グループの生産体制について動画でご紹介
原薬のリスク管理
東和薬品は、1つの原薬に対して複数の原薬メーカーから調達する取り組み(複数購買化)を進め、安定供給の維持に努めています。また、グループ会社の大地化成において原薬を製造(自製化)することで、原薬のさらなる安定確保に向けた取り組みを進めています。原薬メーカーに対しては、「GMP(医薬品及び医薬部外品の製造管理及び品質管理の基準)」を含む薬機法に則った製造がなされているか、安定供給に課題がないかを定期的に調査・確認を行い、恒常的に製品の安定供給を行えるように管理しています。

高い生産能力を備えた3工場による安定した生産体制
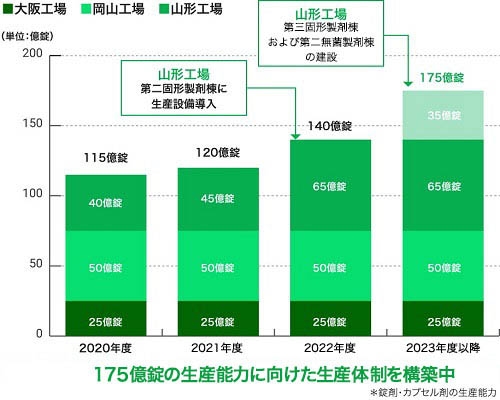
東和薬品は、ジェネリック医薬品メーカーとしての安定供給責任を果たすために、また今後のシェア拡大に対応するべく、生産能力増強のための建設工事を進めました。大阪、岡山、山形に生産拠点を設け、3工場合わせて年間140億錠の生産体制を整えました。さらなる需要増に対応するため、2023年11月に竣工した山形工場の第三固形製剤棟へ導入した全ての設備の立上げバリデーションが完了し、2025年度に年間175億錠の生産能力を有する生産体制を構築しました。
東和薬品では「製品在庫管理者」を設けて社内在庫管理を行うとともに、各工場の生産管理課長を責任者として工場在庫の管理を実施しています。 各製剤は2ヶ月の在庫レベルを下回らないように管理するなど、安定供給に必要な生産体制の確保に努めています。
ニトロソアミン類への対応 ~アトモキセチン製剤の安定供給へ~
アトモキセチン製剤を巡っては、他社を含めてニトロソアミン類が検出されたことを受け供給不安が続き、当事者や支援者による署名活動も展開されるなど社会的関心が高まっていました(参考:発達障害当事者協会(JDDA)の取り組み)。
東和薬品では原因究明を進め、原薬および製剤製造工程における空気中の窒素酸化物NOxがニトロソアミンの生成、混入の一因であることを、2023年末に世界で初めて発表しました。その一連の研究の成果として、アトモキセチン製剤の製造において、世界で初めてNOxを極限まで低減させた環境下でアトモキセチン錠を製造し、許容限度値を下回る製剤の製造に成功しました。(ニトロソアトモキセチンの含有量0.097ppm(許容限度値:0.83ppm))*1。
さらに、安心・安全な製剤の増産に向け、製剤製造所として大阪工場に加え岡山工場及び山形工場の追加の承認を2025年12月に、また原薬製造所として東和薬品グループである大地化成の追加の承認を2026年2月に取得しました。
東和薬品は引き続きニトロソアミン類問題の解決に取り組むとともに、安定供給に努めていきます。
アトモキセチン錠・内用液「トーワ」の予定生産量(百万錠・百万mL)
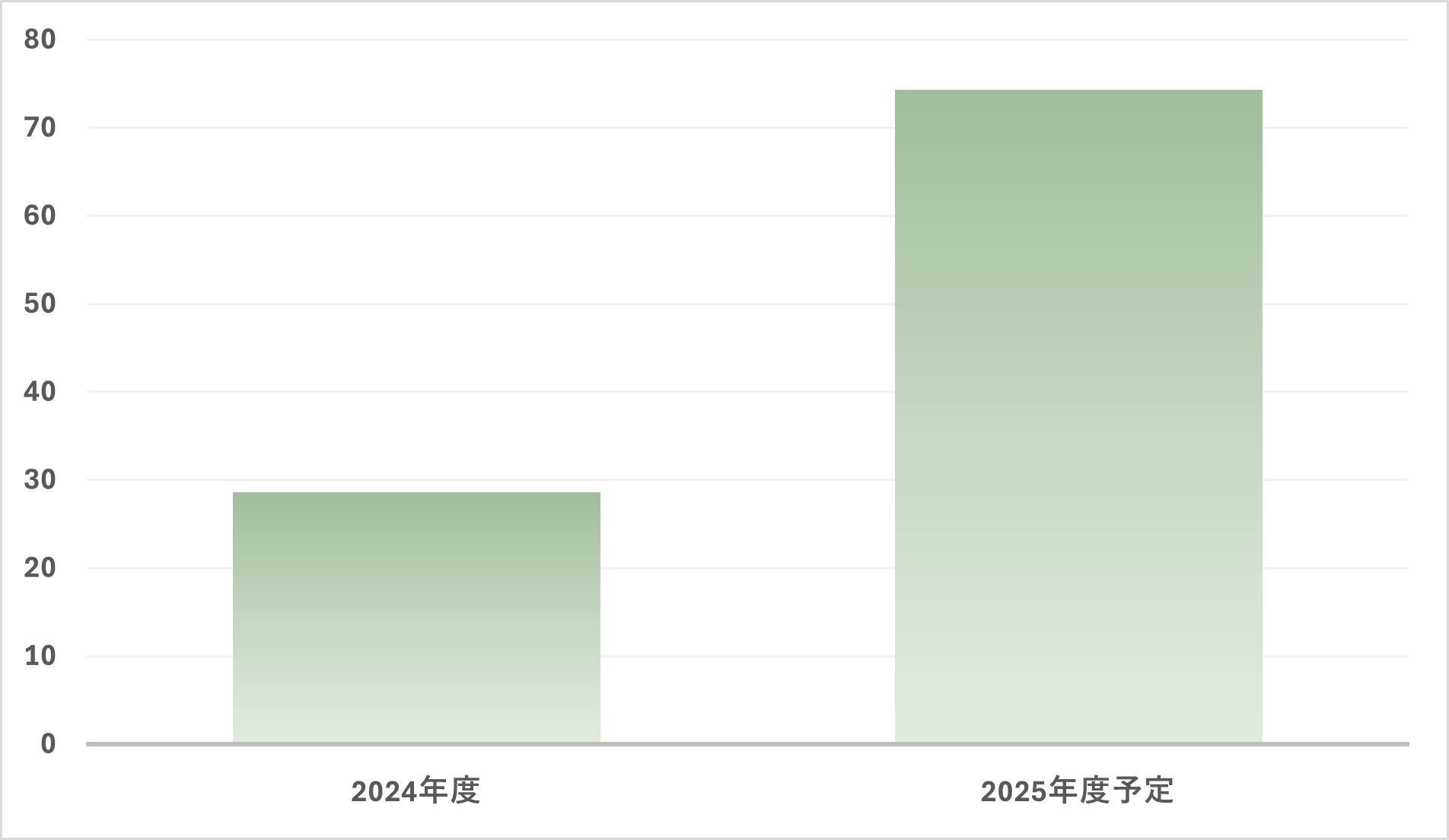
注)3工場(大阪・岡山・山形)での生産体制が整った際の予定生産量を示しています<2025年11月時点予測、グラフは錠(錠数)及び内用液(mL数)の合計>。
また、市場動向や他製品との生産調整等の影響により予定が変わる場合があります。
ニトロソアミン類への対応 ~「東和品質」を守り抜く挑戦~
2018年に、サルタン系製剤(血圧降下剤)に発がん性が懸念されるN-ニトロソジメチルアミン(NDMA)やN-ニトロソジエチルアミン(NDEA)が混入していることが判明し、これを契機にニトロソアミン類の医薬品中への混入について、諸外国と同様に国内でも対応が求められています。厚生労働省から2021年10月8日に「医薬品におけるニトロソアミン類の混入リスクに関する自主点検について」が、その後2025年7月24日に「医薬品におけるニトロソアミン類の混入リスクに関する自主点検後の対応について」が相次いで発出され、継続して適切に管理することが求められています。東和薬品では先進的な独自のアプローチ手法により、リスク低減措置を講じています。
ニトロソアミン類の生成要因と対策
ニトロソアミン類が生成する要因は、大きく分けると以下の2つが考えられます。2021年の通知ではA)を主要因とする低分子ニトロソアミン9種類が挙げられています。その後新たな混入リスクが報告され、B)を生成要因とする原薬が直にニトロソ化されたニトロソアミン類が確認されています。
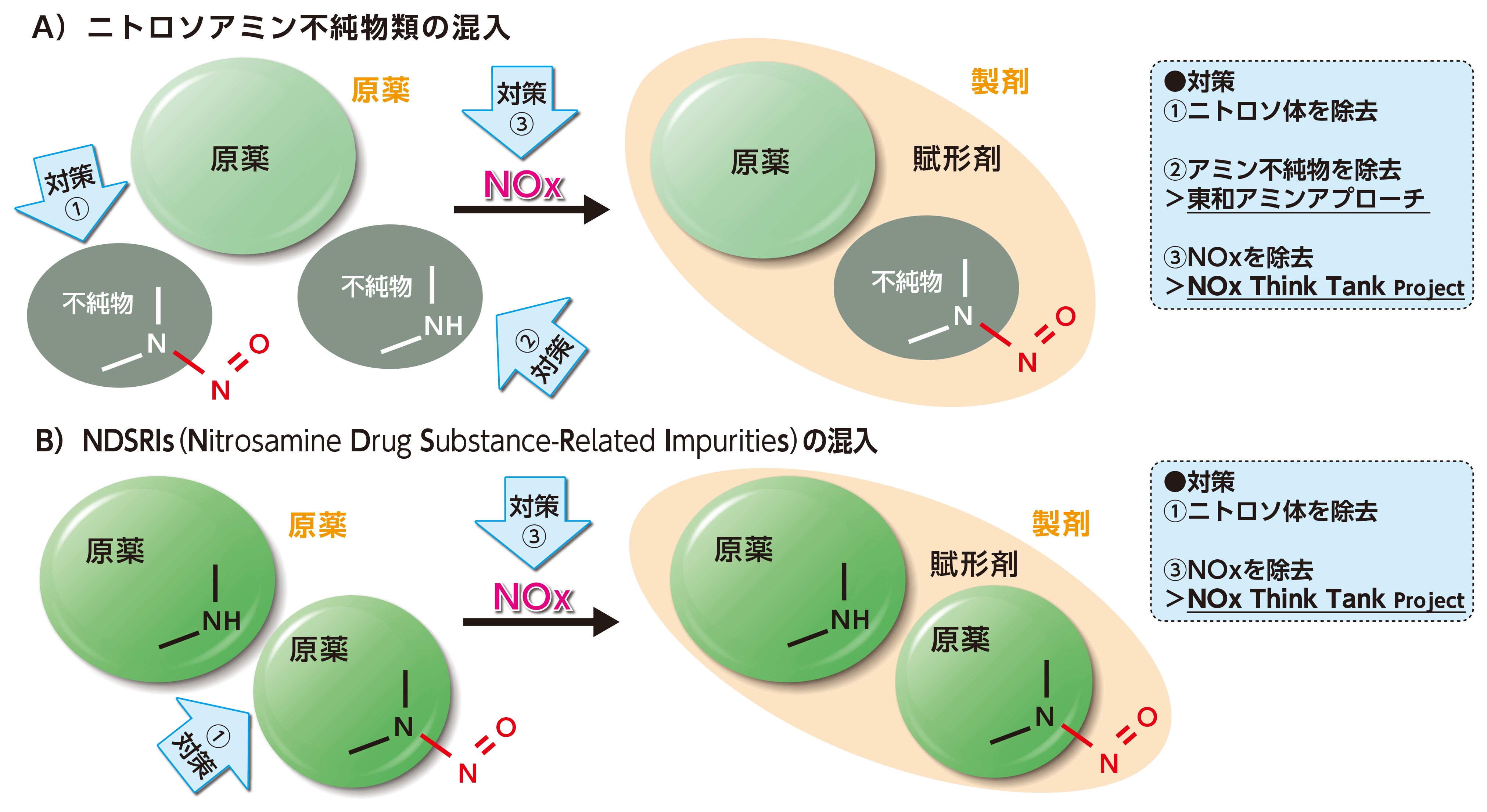

これらの生成要因に着目して、東和薬品では独自のアプローチによる対策を進めています。
東和薬品の取り組み
東和アミンアプローチ
2021年の通知を受け、承認済みの778品目(2021年12月10日現在)ならびに今後開発予定の全品目について、ニトロソアミン類の混入リスクを2023年4月30日までに評価することが求められました。医薬品へのニトロソアミン類の混入リスクを回避するためには、より確実にリスクを評価する取り組みが重要です。 東和薬品では、ニトロソアミン類の生成原因に着目した、“東和アミンアプローチ”を2021年より始動させ、低分子ニトロソアミン類の評価を進めました。
NOx Think Tank Project
●ニトロソアミン類混入の原因を究明
2020年に国内2工場(大阪・山形)で製造されたメトホルミン製剤の一部のロットから暫定基準値を上回るNDMAが検出されたことを受け、原因究明に取り組みました。
最初に原薬製造工程でのNDMA混入を疑いましたが、原薬への混入は認められませんでした。次に製剤化工程に着目し、NDMA混入ロットに紐づく各種データを検証しました。その結果、“同じ原薬・添加物”を使用していたにも関わらず、大阪工場製造品の一部のロットのみ許容摂取値(閾値)を上回るNDMAが検出される事実が判明しました。各種検討の結果、製剤化工程において原薬中に含まれていた極微量のジメチルアミンが空気中の極微量の窒素酸化物NOxと反応し、NDMAを生じたことが判明しました*2。
●ニトロソアミン類混入対策
ニトロソアミン類の生成・混入の一因である空気中の窒素酸化物NOxに着目し、これを低減する方法を模索しました。その結果、空気中の窒素酸化物NOxを効率的に吸着・除去し、ppb レベル(10億分の1)まで低減できる方策を見出しました*3。
詳しくはNOx Think Tank Project(東和薬品コーポレートサイト)に掲載しています。
更なる追究へ
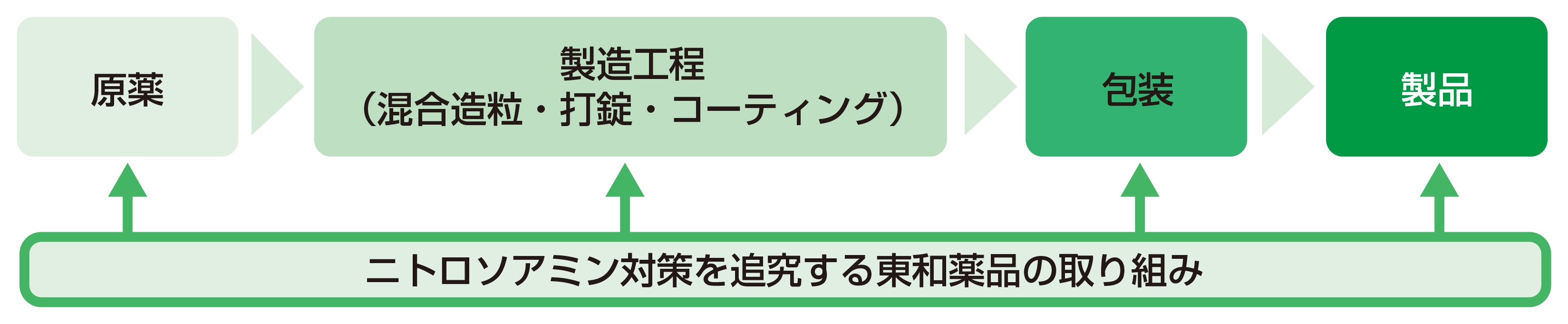
東和薬品はジェネリック医薬品メーカーとして数多くの薬剤を供給し、また新たなジェネリック医薬品の開発を進めています。安心、安全な薬をお届けするため、処方設計の段階から原薬、製造工程、包装、製品に至る包括的なアプローチにより、ニトロソアミン類の混入リスクを低減するための取り組みを引き続き進めてまいります。
*1 Ryota Nomura, Takahiko Taniguchi, Koji Kitada, Mamoru Otsuki, Takuma Tamai, Kazuya Suzuoki, Rintaro Yokoi, Kanako Kondo, and Osamu Uchikawa:Organic Process Research & Development.2025;29(9):2259ー2264
https://pubs.acs.org/doi/10.1021/acs.oprd.5c00182
*2 Shohei Fukuda, Kanako Kondo, Shoji Fukumoto, Norimichi Takenaka, Osamu Uchikawa, and Itsuro Yoshida:Organic Process Research & Development.2023;27(11):2123ー2133
https://pubs.acs.org/doi/10.1021/acs.oprd.3c00274
*3 Ryota Nomura, Takahiko Taniguchi, Kazuya Suzuoki, Rintaro Yokoi, Kanenao Akasaki, Kyoko Hirai, and Osamu Uchikawa:Organic Process Research & Development.2025;29(1):66ー70
https://pubs.acs.org/doi/10.1021/acs.oprd.4c00301
注射剤及び高薬理活性製剤の製造
注射剤の製造
山形工場では、固形製剤に加え、無菌製剤であるアンプル、バイアル、シリンジの製造を行っています。
注射剤の製造において要求される非常に高い無菌性を充填室の全アイソレータ化によって実現しています。更に、バイアル、シリンジの製造ラインは高薬理活性製剤の製造にも対応しています。原材料を受け入れる段階から製造、包装に至るまで、新薬と同様のGMPやGQPなどの厳重な基準に適合していることを確認し、徹底した品質管理を行っています。
ボルテゾミブ注射用3mg「トーワ」
高薬理活性製剤への取り組み
山形工場では、抗がん剤等の高薬理活性製剤も製造しています。
高薬理活性物質は少量でも摂取すると人体に強い薬理活性や毒性を与えるため、製剤製造現場では作業者の安全を確保し、交差汚染を避け、また環境汚染への配慮が必要となります。そのため、封じ込め対策が重要となりますが、より安全に製造するため、山形工場では専用の製造設備を導入し、さらに、一般製剤と隔離されたエリアで製造しています。
薬物漏出防止策の一例
- 保管室、作業室、試験エリアの陰圧制御
- 排気配管は単独の物を使用し、ダブルHEPAフィルタを設置
- 原料及び資材は双方向ではなく一方向による持ち出しを徹底
- 製造後の原料、中間製品を室外へ搬出する際は、容器表面を清浄後、カバーをし、専用ポートを経由して搬出
- 廃棄物は湿潤化させ密閉し、失活処理後に廃棄
- 包装工程でのグローブボックスの使用

グローブボックス
レナリドミドカプセルの製造
レナリドミドは原薬が催奇形性を有しており、高薬理活性物質の中でもより慎重な対応が求められます。
東和薬品では、東和品質の製品をお届けするため、自社製造にこだわり、専用のエリアで製造、かつ入室者を限定することで徹底した薬物漏出防止と作業者の安全対策に努めています。
現場経験豊富なスタッフが設計段階から関与し、安全性を考慮した作業動線や資材の運搬方法を取り入れています。また、電子指図書を導入することで交差汚染や作業ミスのリスクを低減しております。
さらに、製造及び試験エリアで作業するスタッフは曝露による人体への影響を排除するため、装備と教育の面から徹底した対策を行っています。本製剤を取り扱う作業者は過去1年以内にレナリドミドを使用した製剤の取扱いに関する教育、およびSDS教育*を受講した者に限定し、入室時は防護服のみならずエアラインスーツの着用を義務付けています。
*化学物質を取り扱う労働者を対象に、適切な取り扱いをできるように事業者が行う教育


生産バックアップ体制
災害に備えた、バックアップ体制
安定的な製品の供給に向けて内服剤の生産拠点を3工場に分散、注射剤の生産は免震構造を採用した山形工場に集約し、災害リスクを最小限にとどめるよう努めています。万一災害などでどこかの工場が操業を停止した場合にも他の2工場で3シフト体制を敷き、通常時の生産能力を確保するバックアップ体制を構築中です。先進の設備を誇る3工場が、高い品質と安定的な供給を実現し、信頼の未来を支えます。
グループシナジー実現への取り組み
東和薬品は、2020年にスペインのPensa Investments, S.L.(現商号:Towa Pharma International Holdings, S.L.、以下「Towa INT」)を子会社化しました。
Towa INTは、欧州や米国を中心に、世界40か国を超える国や地域で210成分以上のジェネリック医薬品を提供しています。
また東和薬品では、グループシナジー実現に向けた取り組みを進めております。
その一つの成果として、エソメプラゾールカプセル10mg/20mg「トーワ」の製造所の追加に関する一部変更承認申請を行い、2024年2月に承認を取得いたしました。
今回新たに追加された製造所は、Towa INTの傘下のTowa Pharmaceutical Europe, S.L.がスペインで運営するマルトレージャス工場です。マルトレージャス工場は、EMA(欧州薬品庁)やFDA(アメリカ食品医薬品局)の基準に準拠した製造拠点で、今回新たに日本市場に向けた製品製造の承認を受けました。
承認取得後速やかに製造を開始し、2024年3-4月から製品の市場出荷を行っています。

 Towa Pharmaceutical Europe, S.L.
Towa Pharmaceutical Europe, S.L.マルトレージャス工場
マルトレージャス工場では大型造粒機を用いた大量かつ効率的な生産という強みを活かし、欧米の市場に製品を提供してきました。この度、日本市場に向けた製品を製造することで、グループとしての生産バックアップ体制の強化につなげるとともに、現在課題となっている国内の安定供給へ貢献していきます。これはTowa INT子会社化後のグループシナジーの一つの成果であり、今後、グループ各社の技術を活かした共同開発など更なる事業強化に努めていきます。
東和薬品の生産体制(動画)
物流の効率化と物流機能のバックアップ体制
各工場から出荷された製品は東日本物流センター(山形)、西日本物流センター(岡山)に保管されます。この東西物流体制は、安定供給のために非常に重要な役割を担っています。万一、災害などの理由によりいずれかの物流センターが稼動停止になった場合でも、もう一方の物流センターから日本全国へ製品をお届けすることが可能です。また、関東出荷センター(茨城)、関西出荷センター(兵庫)を開設し、取り扱い物流量の増加に対応するなど、安定供給体制の維持・強化を図っています。
 東日本物流センター
東日本物流センター 西日本物流センター
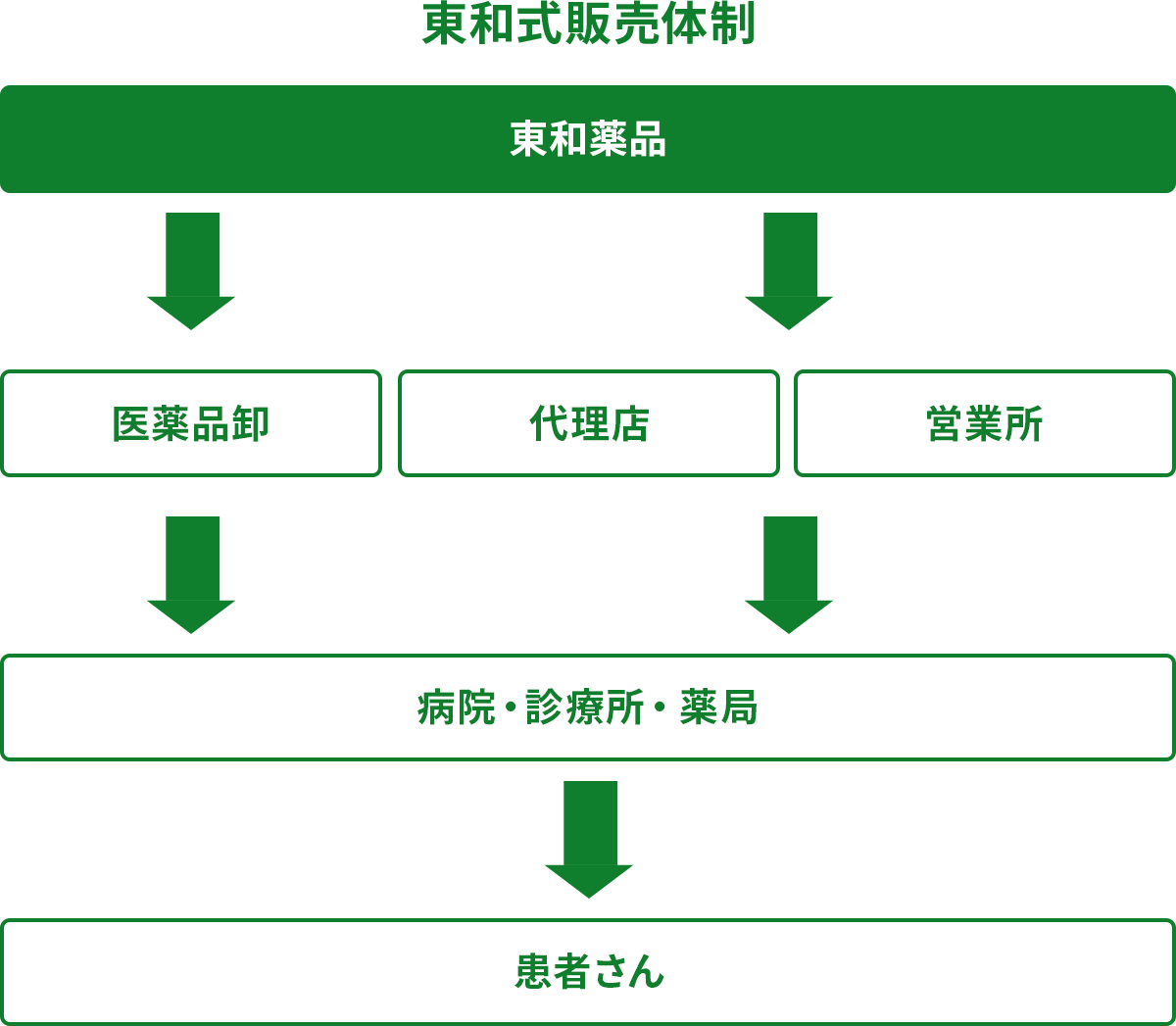
西日本物流センター医療機関のニーズに沿ってお届けする「東和式販売体制」
東和薬品では、全国の営業所や代理店を拠点として直接医療機関へお届けする直販体制と 医薬品卸売業者を通じてお届けする2つの販売体制を敷いています。 これは、全国の医療機関のニーズに沿って弊社製品をお届けできる体制です。また、ジェネリック医薬品業界最多のMRが情報提供・収集を行い 医療現場の要望を迅速に社内へフィードバックできる体制でもあります。今後も、きめ細かな対応により、付加価値の高いジェネリック医薬品を着実に届け続けられるよう努めていきます。
 医療関係者向けサイト
医療関係者向けサイト



